
Introduction
糖尿病已成为一个在全球范围内迅速蔓延的健康难题,约 9.5% 的世界人口受其影响。国际糖尿病联盟(IDF)《糖尿病地图》第 10 版指出,糖尿病会引发多种身体系统的并发症,显著增加早死风险。糖尿病足溃疡(DFU)作为糖尿病的一种并发症,约四分之一的糖尿病患者会发展为此病症。糖尿病足问题极大地提升了发病率与死亡率,其主要特征为伤口愈合延迟。影响糖尿病伤口愈合的因素众多,涵盖生长因子生成受阻、胶原蛋白积累异常,以及角质形成细胞迁移和增殖受影响等。因而,探究改变的伤口愈合机制,对改善 DFU 的治疗效果至关重要。
Notch 信号通路是一种广泛存在且在进化上高度保守的细胞内信号途径,调控着多种细胞功能,在细胞增殖、凋亡 / 存活以及血管生成等过程中发挥关键作用。诸多研究已证实 Notch 与皮肤稳态密切相关。该信号通路维持着角质形成细胞生长停滞与渐进性分化过程的平衡,还能促进角质形成细胞的增殖。在正常伤口愈合进程中,Notch 信号对细胞迁移和炎症反应起正向调节作用。然而,在糖尿病状态下,Notch 信号过度激活,反而阻碍了伤口愈合。高血糖引发的 Notch1 信号激活,延迟了角质形成细胞的迁移,对糖尿病患者的伤口愈合造成显著损害。这些发现表明,针对 Notch1 信号或许是治疗糖尿病伤口的潜在策略。
Results
一、靶向高糖病理微环境的发现
在过往研究中,伤口愈合研究多聚焦于正常生理环境,而本研究聚焦糖尿病病历条件,证明了表没食子儿茶素 - 3 - 没食子酸酯(EGCG)能够在高糖条件下逆转细胞迁移抑制效应。利用糖尿病小鼠模型进行验证,结果显示,经 EGCG 处理后,伤口愈合率显著升高(见图 2)。这一成果充分表明,EGCG 在病理状态下相较于正常生理环境,具备更为显著的治疗优势。
二、Notch 信号通路调控机制深入解析
本研究以创新视角,深入揭示了 EGCG 独特的 “受体 - 效应器” 双级调控模式。具体表现为:一方面,EGCG 可直接抑制 Notch1 受体的激活,致使 NICD 表达水平降低(见图 1C);另一方面,能够下调关键下游效应分子 Hes - 1(见图 5C)。尤为重要的是,本研究在表皮细胞中建立了 EGCG - Notch1 - Hes - 1 信号轴与细胞功能调控之间的直接联系,并通过图 4 的双重染色实验得以验证。
三、多功效协同促愈作用模式的发现
本研究深入剖析,揭示了 EGCG 独特的三维修复机制。其一,EGCG 能够有效促进表皮细胞迁移,使细胞在 48 小时内的迁移率显著提高;其二,可激活细胞增殖,让 Ki - 67 阳性细胞数量大幅增加(见图 3F);其三,能够调控细胞外基质(ECM)重构,使胶原沉积量增加。这种迁移、增殖与基质重塑之间的协同效应,为糖尿病创面治疗开辟了全新的策略路径。
Discussion and Conclusion
糖尿病患者常因多种因素致伤口愈合延迟,细胞损伤影响再上皮化与真皮重塑,慢性伤口边缘角质形成细胞迁移受阻,阻碍小鼠愈合进程。随着糖尿病患者增多,慢性不愈合伤口发生率上升,亟需新疗法加速角质形成细胞迁移、增强再上皮化、促进伤口闭合。
本研究发现,EGCG 可靶向 Notch 增强角质形成细胞再上皮化,改善糖尿病小鼠伤口愈合。角质形成细胞是皮肤主要细胞,在伤口愈合中起关键作用。糖尿病伤口中,生物机制破坏致角质形成细胞功能障碍,迁移和增殖受损,导致愈合不良。本研究显示,糖尿病小鼠表皮细胞增殖受抑,上皮化延迟,与先前研究一致。本研究还确定 Notch 途径是糖尿病小鼠伤口愈合时抑制表皮细胞增殖的新机制。
Notch 信号通路协调表皮增殖,高糖条件下 Notch 信号激活依赖 γ- 分泌酶介导的受体切割。本研究证实,高糖可激活 Notch,体外 NICD 水平增加,糖尿病小鼠皮肤中也检测到 Notch 激活,凸显其在糖尿病伤口愈合中的重要作用,提示其可作为治疗靶点。此前研究表明抑制 Notch 信号可改善糖尿病伤口愈合,本研究发现 EGCG 通过抑制 Notch 加速表皮增殖、改善上皮化。
本研究利用永生化人类角质形成细胞模型,证实 EGCG 可抑制高糖诱导的 Notch 信号过度激活,动物实验也显示 EGCG 加速糖尿病小鼠伤口皮肤表皮增殖、抑制 Notch 信号通路。总之,本研究表明 EGCG 靶向 Notch 途径促进糖尿病小鼠上皮化、增强伤口愈合。研究开创性地将植物多酚治疗手段与糖尿病创面微环境调控策略相结合,为后续开发靶向 Notch 通路的局部给药系统奠定了坚实的理论基础。
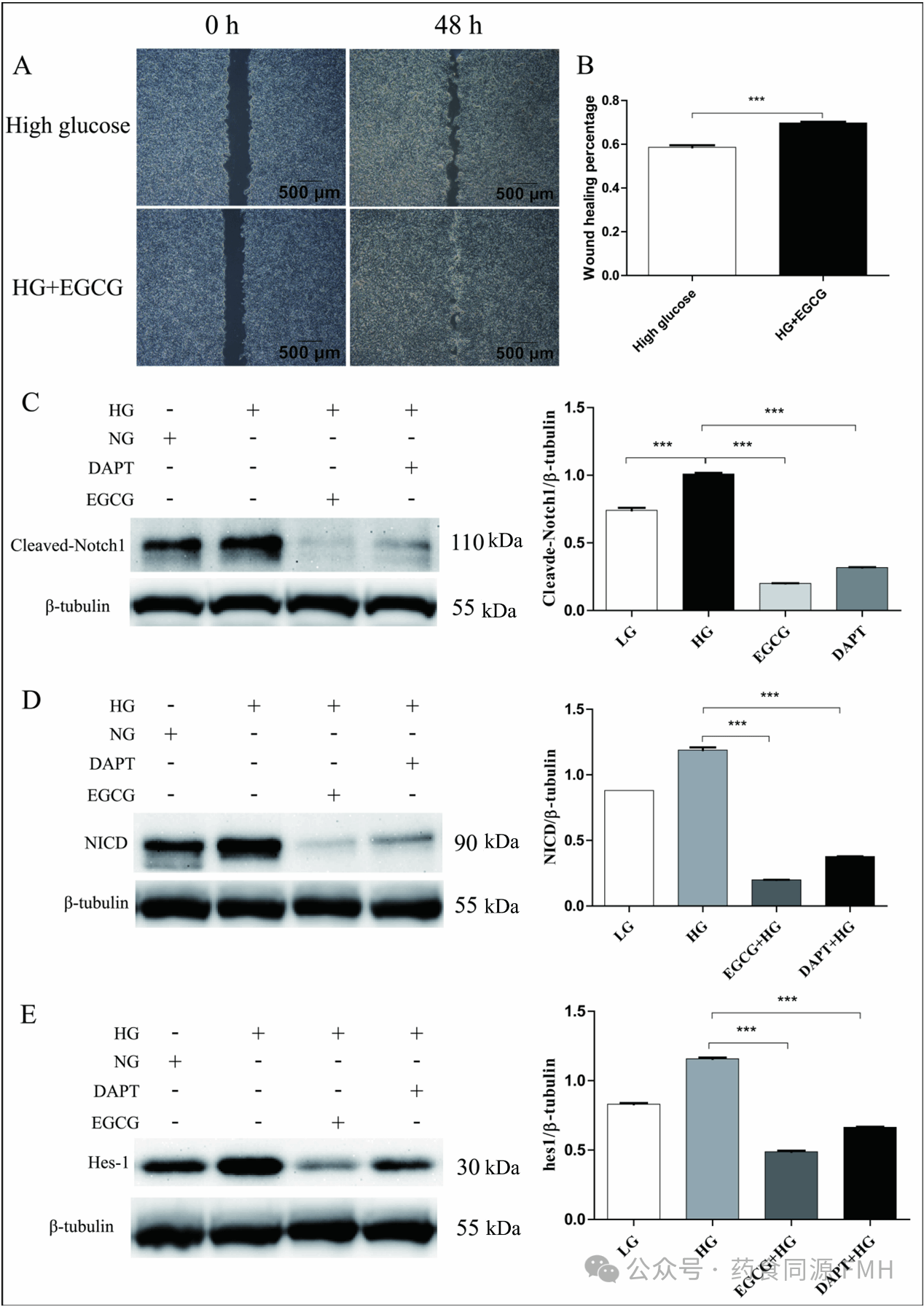
图1 EGCG通过靶向Notch信号通路增强人角质形成细胞的迁移能力
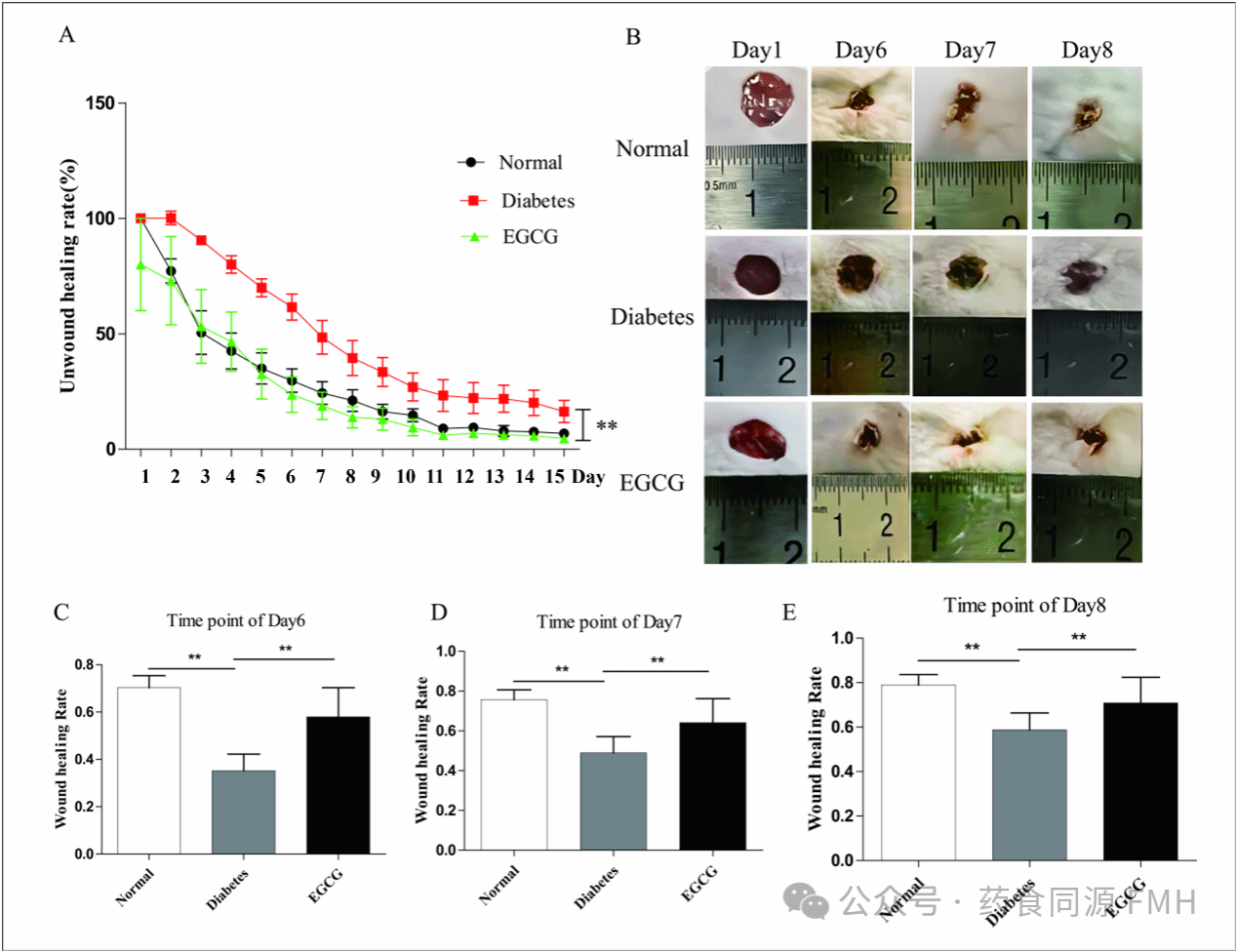
图2 EGCG可以改善糖尿病小鼠的伤口愈合
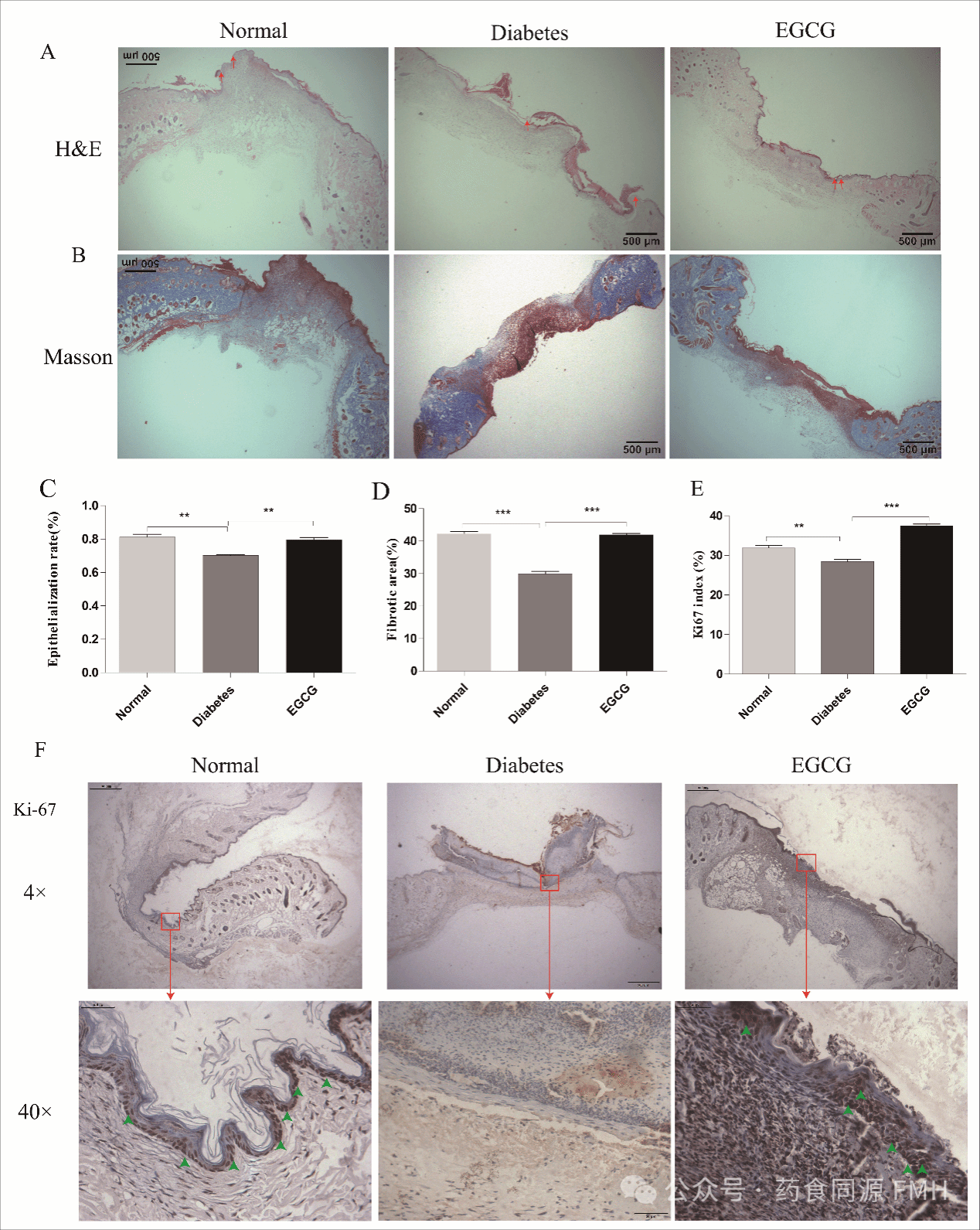
图3 EGCG能够加速再上皮化、胶原沉积和表皮细胞增殖
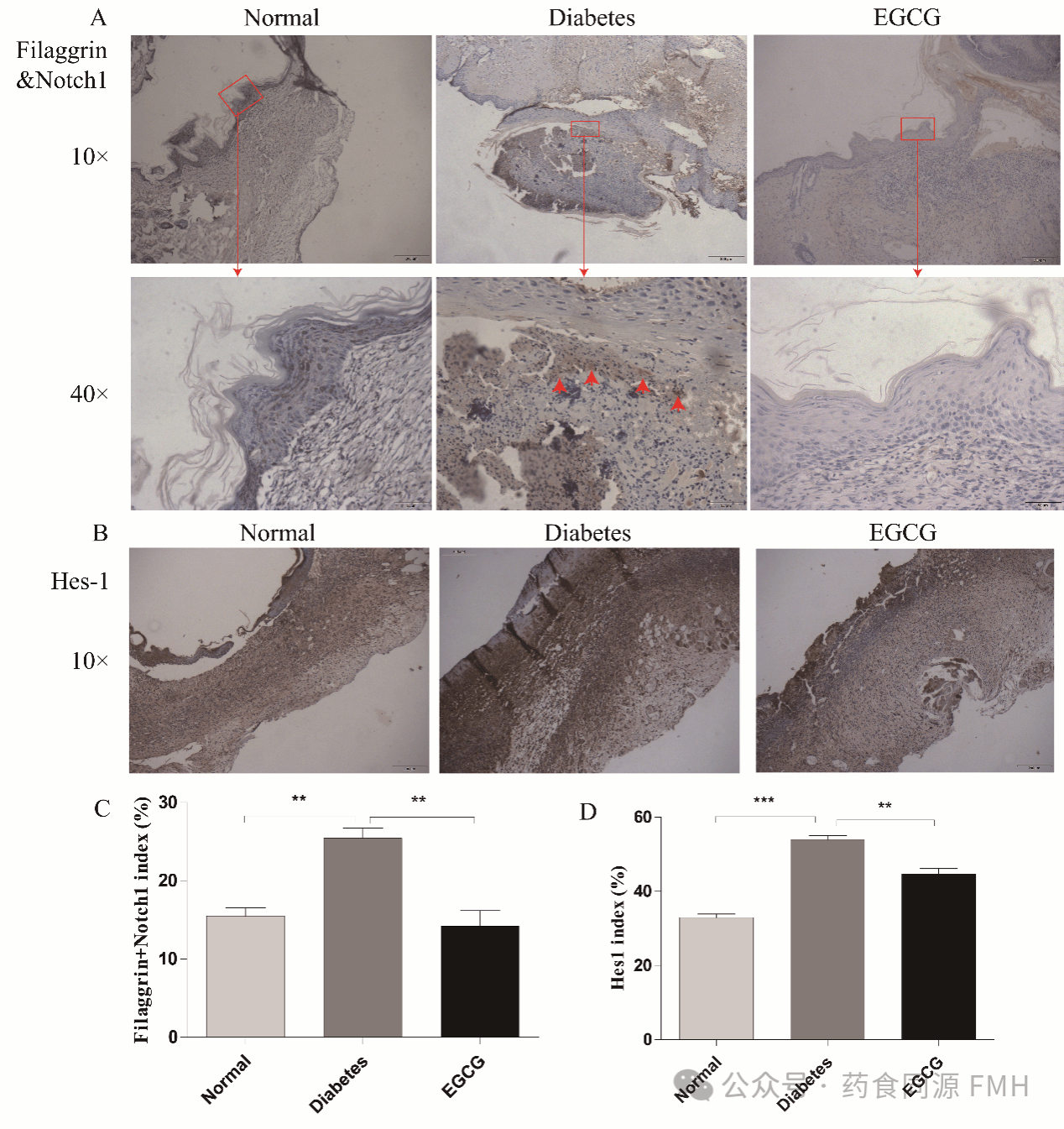
图4 EGCG调节糖尿病表皮中的Notch信号通路
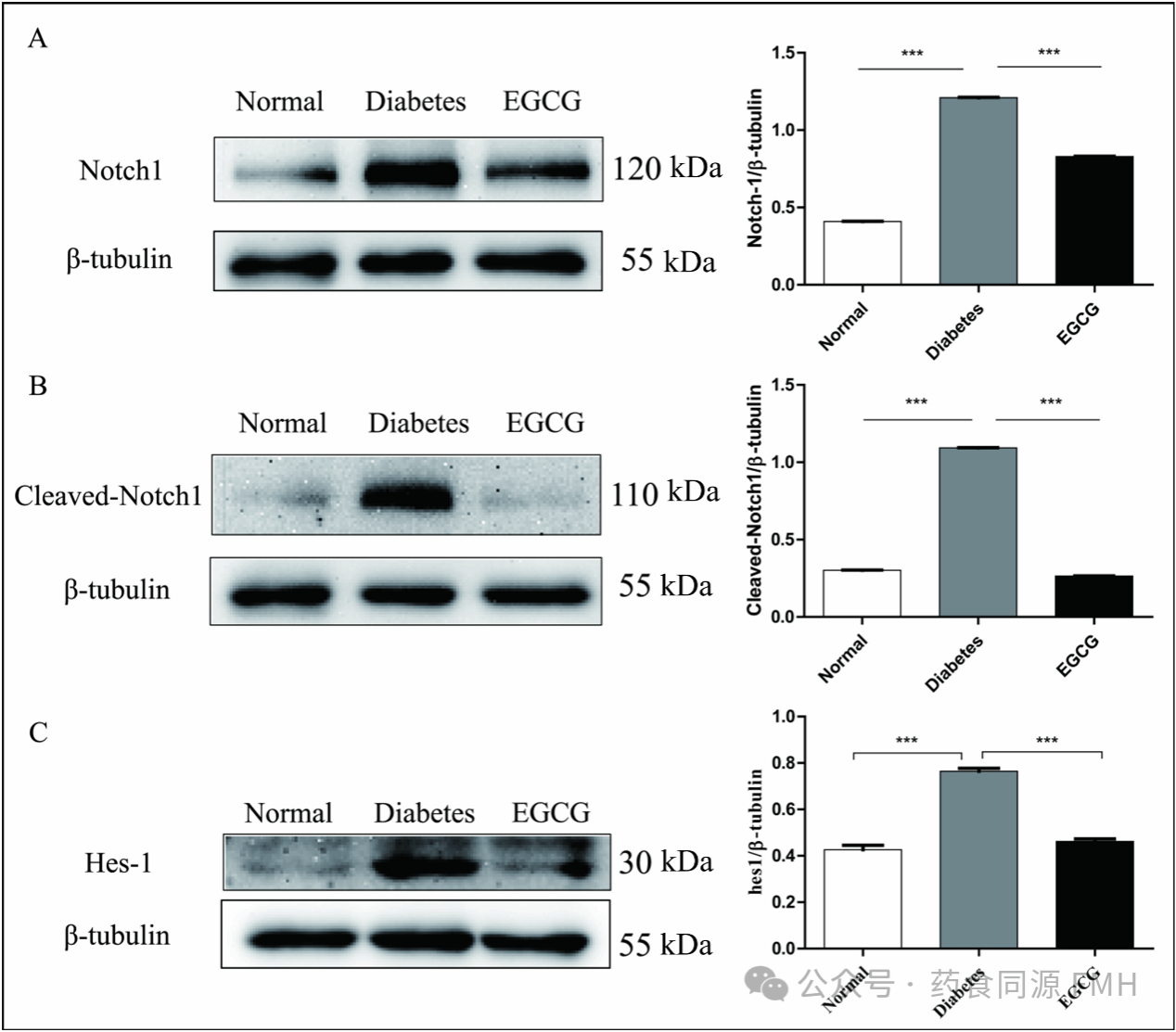
图5 EGCG在糖尿病小鼠中抑制了Notch信号通路
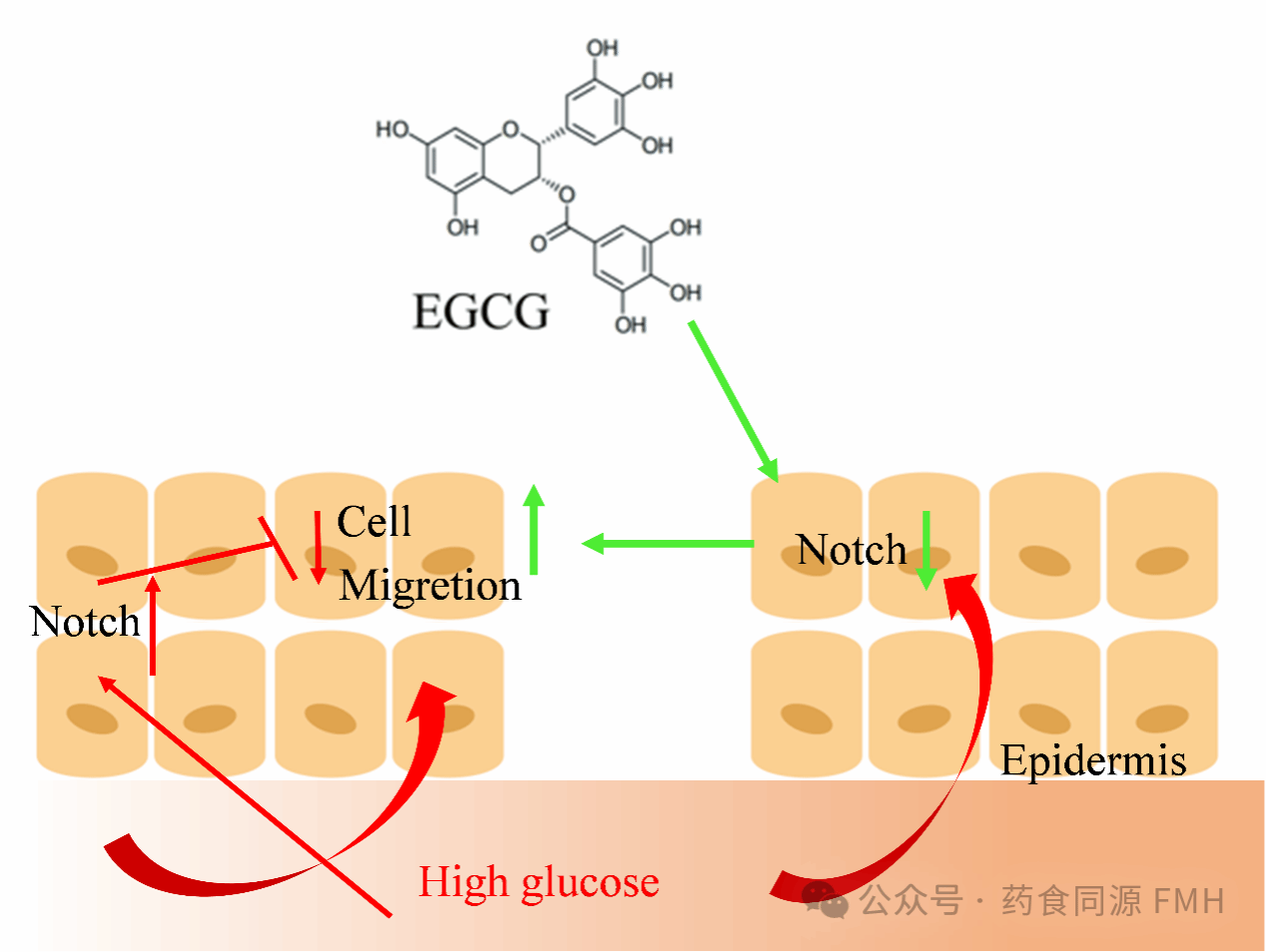
图6 EGCG通过靶向Notch信号通路加速糖尿病小鼠的表皮迁移
作者简介
第一作者

蒋蝶,女,云南农业大学食品科学技术学院在读硕士,主要研究方向为天然产物活性研究、食品资源营养与健康。

朱强强,博士,讲师,云南农业大学食品科学技术学院、普洱茶学教育部重点实验室、食药同源资源开发与利用教育部工程中心、云南省精准营养与个性化食品制造重点实验室研究骨干,长期从事食药资源功效作用及功能机理解析、精准营养食品开发制造和成果转化等工作,在植物基食品功效作用及功能活性成分解析、精准营养产品上取得系列成果,创新集成食品开发系统,形成以功能成分包被、功效验证、产品研发为一体的精准营养食品研制体系,研制系列新产品。主持省部级项目3项,申报专利5件,现以第一/通讯作者(含共同)身份发表论文12篇。2024年获云南省科技副总聘任人选,聘任云南省品斛堂生物有限公司研发副总。
通信作者

徐欢欢,男,博士,副教授,硕士研究生导师,云南省“兴滇英才支持计划”青年人才,研究方向为食药资源开发与利用,疾病方向集中于关节炎、骨质疏松、皮肤光老化、衰老、肿瘤等,作为负责人构建了天然化合物实体库(大于3600个),能熟练运用分子互作技术(SPR/BLI/ITC)进行相关药物筛选及开发,主持国家自然科学基金青年基金1项、省部级项目5项,现以第一/通讯作者(含共同)身份发表SCI收录论文26篇,授权实用新型专利4件,申报发明专利4件。

盛军,二级教授,日本大阪大学博士,原卫生部长春生物制品研究所所长、云南农业大学原校长、云南省高原特色农业产业研究院原院长;现任中国微生物学会常务理事,云南省微生物学会理事长,教育部高等学校教学指导委员会委员。长期从事食药资源组学研究、功能机理解析和成果转化,在植物基食品组学、功能活性成分解析以及精准营养产品上取得系列成果。破译特色植物资源基因组,构建了国际上首个食药同源资源跨组学数据;创建跨界物种植物多酚生物合成大数据,揭示植物基食物多酚调节代谢免疫机制。建立了植物基功能组分定向发酵富集技术,创新集成工艺装备,建成普洱茶、石斛、辣木、核桃等深加工技术体系,研制系列新产品,并实现产业化推广应用,产生了显著的经济效益和社会效益。获授权专利73件,发表论文309篇(SCI论文160篇),以第一或通讯作者在SCIENCE、Nature Communications、Molecular Plant等杂志上发表论文138篇,出版学术著作4部。获吉林省科技进步一等奖,云南省科技进步一等奖,云南省科技进步特等奖,云南省科学技术杰出贡献奖,世界茶业大会普洱茶特别贡献奖;入选云南省科技领军人才,首批国家跨世纪百千万人才工程国家级人选,全国优秀科技工作者。
原文链接:https://www.sciopen.com/article/10.26599/FMH.2027.9420144
扫码关注我们!
