
Introduction
中药是丰富的天然化学库,蕴含着多种具有生物活性的化合物,乌药作为其中的典型代表,是一种珍贵的药食两用物质。乌药原植物主要分布于中国长江流域以南地区以及日本和东南亚。乌药药用部位为根,使用历史源远流长,而叶片在本草中亦有记载,常用于治疗急性蜂窝组织炎、痈肿、胃炎和风湿性关节炎等疾病。2014年,乌药叶被正式列为新资源食品,因其降脂功效而被广泛制成茶饮。然而,乌药叶中具体的降脂活性成分及其作用机制尚未完全明确,亟待深入的科学研究加以探索。
传统天然活性化合物的筛选方法存在效率低下、程序繁琐、耗时长和成本高昂等不足。近年来,研究发现将靶蛋白固定于固体载体上进行配体捕获,是一种高效的活性成分筛选策略。沸石咪唑盐框架-8(ZIF-8)凭借其类似沸石的晶体结构、小孔径、大比表面积以及卓越的稳定性和生物相容性,成为理想的酶固定材料。通过仿生矿化法将脂肪酶固定在ZIF-8上,不仅简化了实验步骤、降低了成本,还显著提高了酶的可重复使用性、催化活性和稳定性。然而,目前尚无将脂肪酶-ZIF-8杂化反应器用于天然植物或中药中脂肪酶抑制剂筛选的研究报道。
浙江工业大学楚楚教授团队建立了一种高效可靠的活性化合物筛选策略用于乌药叶中脂肪酶抑制天然活性成分的快速辨识。首次将脂肪酶-脯氨酸-金属有机框架(PPL@ZIF-8)杂化固定化酶微反应器结合HPLC-Q-TOF-MS/MS,从复杂体系中快速筛选天然脂肪酶抑制剂,并进一步通过分子对接与分子动力学模拟技术探究活性成分与酶的相互作用,初步阐释活性成分脂肪酶抑制的潜在机理。
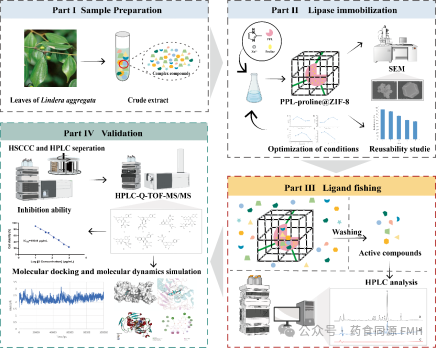
图1 基于HPLC-Q-TOF-MS/MS和分子对接技术,用酶-ZIF-8杂化反应器快速筛选与鉴定乌药叶中潜在脂肪酶抑制剂示意图
Results and Discussion
1. 脂肪酶-脯氨酸-金属有机框架杂化反应器(PPL@ZIF-8)的合成
在脯氨酸辅助的条件下,通过一锅法制备,将脂肪酶固定在ZIF-8金属框架上。采用傅立叶变换红外光谱、X射线粉末衍射、扫描电子显微镜等材料表征技术,证明了脂肪酶金属有机框架微反应器成功合成(图2)。以考马斯亮蓝法测定固定化酶的负载率,及(图3),探究了最佳的杂化反应器合成条件(图4)。

图2 ZIF-8和PPL@ZIF-8的表征。(A)游离脂肪酶 (a)、PPL@ZIF-8 (b)和脯氨酸-ZIF-8 (c)的FT-IR光谱;(B)ZIF-8和PPL@ZIF-8的PXRD图谱;(C)ZIF-8和PPL@ZIF-8在不同的放大倍数下的SEM图像(每个图像中显示的放大倍数)
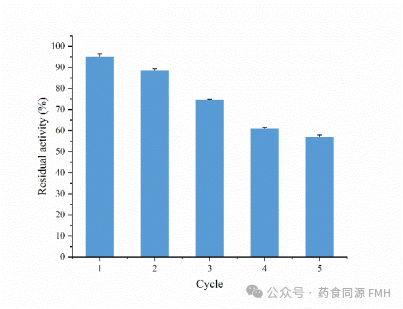
图3 PPL@ZIF-8的可重复使用性研究
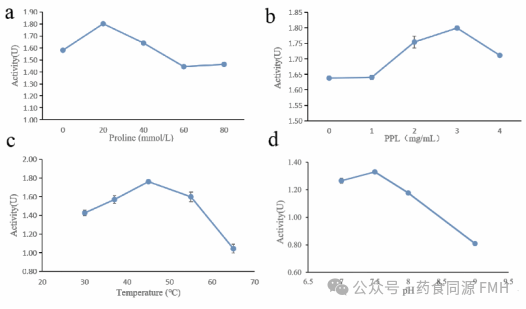
图4 脯氨酸浓度(A)、脂肪酶浓度(B)、温度(C)、pH值(D)对PPL@ZIF-8合成的影响
2. 基于HPLC-Q-TOF-MS/MS鉴定lipase–proline@ZIF-8在乌药叶中快速筛选潜在脂肪酶抑制剂的结果
如图5所示,结合HPLC-Q-TOF-MS/MS分析,初步鉴定出7个潜在脂肪酶抑活性化合物。通过体外脂肪酶抑制活性的测定来检验鉴定结果(表1)。
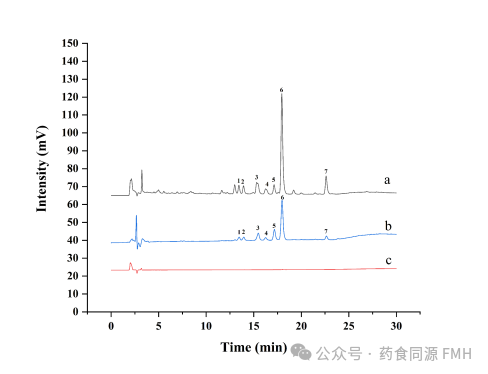
图5 不同阶段的HPLC色谱图。(a)乌药粗提取物;(b)PPL@ZIF-8的筛选结果;(c)第三次PBS洗涤溶液
表1 筛选出的7种化合物的体外脂肪酶抑制活性的测定结果

利用分子对接技术与分子动力学模拟初步探究潜在脂肪酶抑制活性有效成分的作用机理
通过分子对接技术初步探究潜在降血脂活性化合物与脂肪酶结合的构象和优选结合位点,解释其相互作用机制。如表2所示,筛选得到的化合物对脂肪酶表现出很强的亲和力。结合分子对接结果与体外抑制活性的测定结果,选择Quercetin-3-O-β-D-glucoside、Quercetin-5-O-β-D-glucoside、Quercetin-5-O-β-D-glucoside和Kaempferol-7-O-α-L-rhamnopyranoside进行分子动力学模拟研究(图6)。
表2 7种化合物的分子对接结果

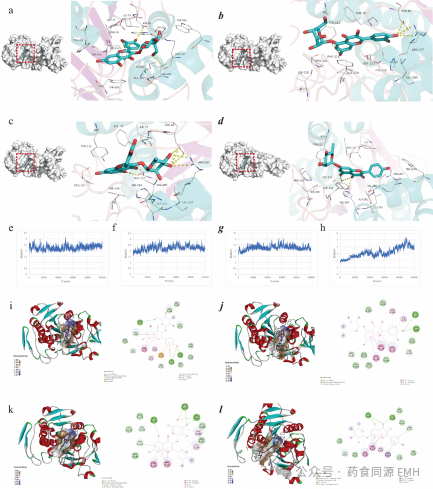
图6 脂肪酶与化合物在活性位点形成的复合物以及分子动力学模拟结果:(A)PPL-quercetin-3-O-β-D-glucoside复合物;(B)PPL-quercetin-5-O-β-D-glucoside复合物;(C)PPL-quercetin-3-O-α-L-rhamnopyranoside复合物;(D)PPL-kaempferol-7-O-α-L-rhamnopyranoside复合物;(E)PPL-quercetin-3-O-β-D-glucoside复合物的RMSD结果;(F)PPL-quercetin-5-O-β-D-glucoside复合物的RMSD结果;(G)PPL-quercetin-3-O-α-L-rhamnopyranoside复合物的RMSD结果;(H)PPL-kaempferol-7-O-α-L-rhamnopyranoside复合物的RMSD结果;(I)quercetin-3-O-β-D-glucoside的氨基酸相互作用;(J)quercetin-5-O-β-D-glucoside的氨基酸相互作用;(K)quercetin-3-O-α-L-rhamnopyranoside的氨基酸相互作用;(L)kaempferol-7-O-α-L-rhamnopyranoside的氨基酸相互作用。
Conclusion
本研究成功开发了一种新型的基于脂肪酶杂化ZIF-8反应器的筛选策略,高效筛选出乌药叶中7个天然脂肪酶抑制剂,其中4个成分Quercetin-5-O-β-D-glucoside、Quercetin-3-O-α-D-xyloside、Quercetin-3-O-α-L-arabinofuranoside和kaempferol-7-O-α-L-rhamnopyranoside被首次报道具有脂肪酶抑制活性。该固定化策略提高了脂肪酶的再使用性能,使酶具有更好的储存稳定性和热稳定性,拓宽了酶在天然活性成分筛选中的应用,为挖掘更多潜在活性分子开发新药提供了宝贵的技术支撑。更重要的是,这项研究为未来乌药在降脂方向保健食品和药品的进一步开发奠定了科学的基础。
作者简介
第一作者

张馨丹,女,浙江工业大学药学院硕士,主要研究方向为中药药效物质研究。参与浙江省尖兵领雁项目,发表sci论文3篇。
通信作者

楚楚,女,浙江工业大学药学院教授,博士生导师,博士后合作导师,现任浙江工业大学药学院副院长。中国中西医结合学会中药专委会委员;世中联中药分析专委会委员;中华中医药学会中药分析分会委员;浙江省中西医结合学会中药专委会委员;浙江省毒理学会中药与化妆品安全性专委会青年副主任委员;浙江省营养学会中医药养生与营养专委会青年副主任委员;浙江省药学会中药与天然药物专委会青年委员。长期从事中药活性成分筛选及产品开发、中药质量标准方向研究工作。主持承担国家自然科学基金面上项目(2项)、青年基金、浙江省自然科学基金等科研项目20项。承担质量标准起草10余项,被中国药典、美国药典等收录。发表SCI论文60余篇,第一发明人获授权发明专利17项,获第二届省自然科学奖三等奖、省药学会科技奖二等奖。
原文链接
https://www.sciopen.com/article/10.26599/FMH.2026.9420097