
Introduction
糖尿病慢性创面(尤其是糖尿病足溃疡)是糖尿病最棘手的并发症之一。由于持续的炎症反应、氧化应激损伤、血管再生障碍及细菌感染风险,这类创面愈合缓慢、易感染、复发率高,给患者生活质量和医疗系统带来巨大负担,已成为临床上面临的重大挑战。传统治疗手段难以同时应对这些复杂的病理微环境,亟需开发新型多功能创面敷料。
姜黄,作为姜科植物姜黄的干燥根茎,既是传统调味品,更是《中国药典》收载的常用中药,具有破血行气、通经止痛之功效。姜黄素(Curcumin)是从姜黄中提取的一种二酮类天然多酚化合物,是姜黄的主要活性成分,也是典型的药食同源功能因子,在亚洲有着数千年的食用和药用历史。姜黄素具有抗氧化、抗炎、抗菌等多种药理活性,在伤口管理领域展现出巨大潜力。然而,姜黄素水溶性差(约11 ng/mL)、生理pH下快速降解(半衰期<10分钟)、口服生物利用度极低(<1%)等缺点严重制约了其临床应用。通过金属离子配位策略,将姜黄素与铜离子(Cu²⁺)络合形成姜黄素-铜纳米颗粒(Cur-Cu NPs),不仅能够改善其水分散性,还可赋予其促血管生成的协同功能——铜离子本身可促进血管内皮生长因子(VEGF)分泌,增强细胞迁移能力。
与此同时,MXene(Ti₃C₂)作为一种新兴的二维过渡金属碳/氮化物纳米材料,具有优异的光热转换效率(本研究中η=24.2%)、广谱自由基清除能力和物理穿刺抗菌性能。将药食同源活性成分姜黄素-铜纳米颗粒与MXene纳米片共同负载于温敏水凝胶基质中,可望实现对糖尿病创面复杂微环境的多维度时空精准调控。
Results and Discussion
2026年3月8日,湖北工业大学生命科学与健康工程学院匡映副教授/李草教授/刘佳教授团队在国际权威期刊《Journal of Nanobiotechnology》(IF:12.6,中科院1区)上发表了题为"Photothermal-responsive MXene/curcumin-copper composite hydrogel with antioxidant, immunoregulatory, and angiogenic functions for diabetic wound healing"的研究论文(论文链接:https://doi.org/10.1186/s12951-026-04189-5)。湖北工业大学廖涛博士为第一作者,湖北工业大学匡映副教授、李草教授及刘佳教授为共同通讯作者。
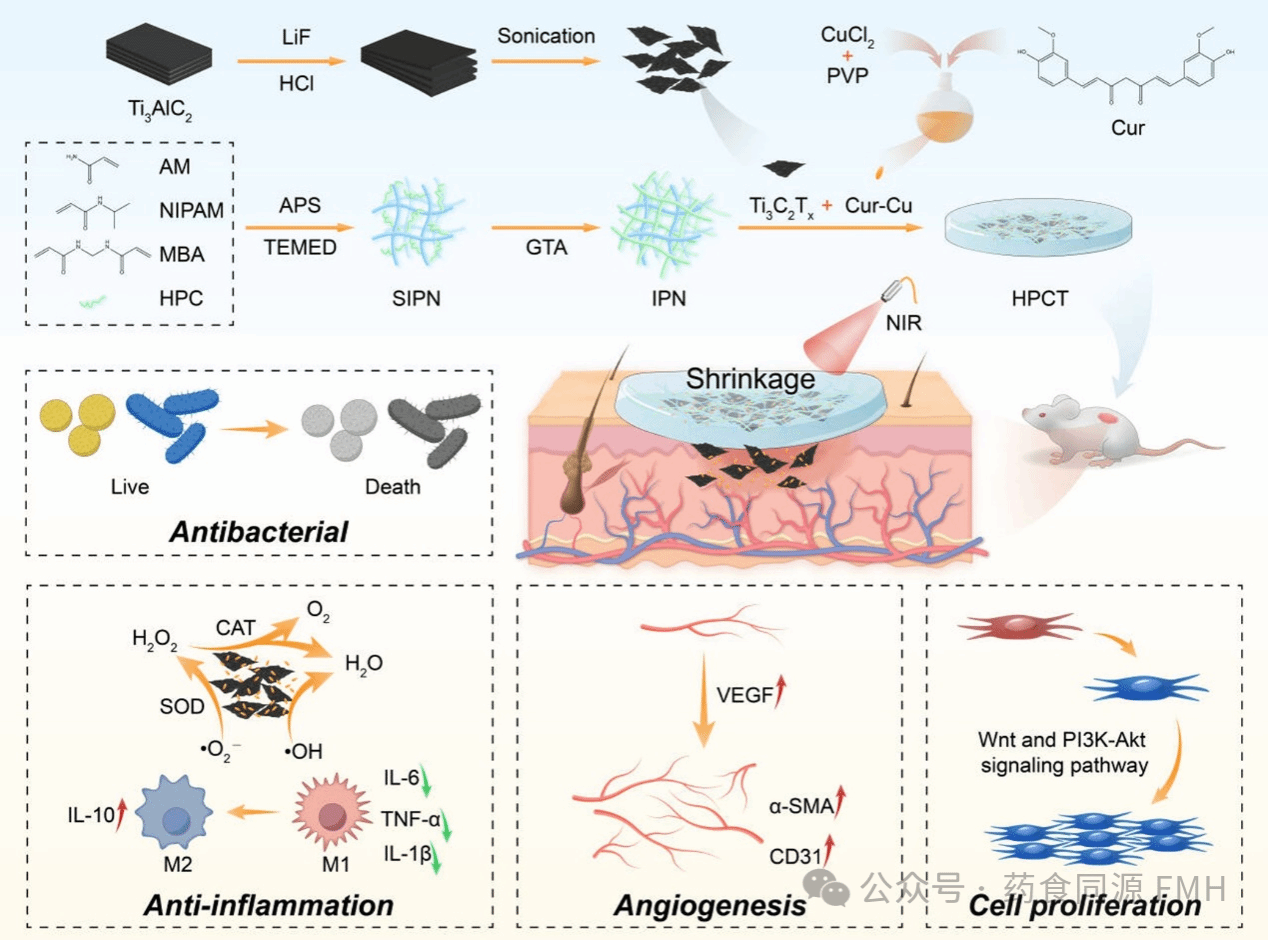
该研究受药食同源理念启发,以姜黄素这一经典药食同源成分为切入点,设计了一种集抗氧化、免疫调控、促血管生成及抗菌功能于一体的光热响应型MXene/Cur-Cu纳米复合水凝胶(HPCT),通过整合二维纳米材料Ti3C2Tx MXene与姜黄素-铜纳米颗粒(Cur-Cu NPs),并嵌入温敏型双网络聚合物水凝胶中,实现多功能协同治疗。
MXene具备优异的光热转换与自由基清除能力,在近红外激光照射下可产生热效应,触发水凝胶收缩,实现药物的可控释放。同时其二维结构还能破坏细菌细胞膜,发挥抗菌作用。另一方面,姜黄素-铜复合纳米颗粒具有良好的抗氧化、抗炎和促血管生成能力,其中铜离子还能刺激血管内皮生长因子表达,从而促进内皮细胞迁移与血管新生。得益于各组分的协同效应,HPCT水凝胶具有优异的理化稳定性、高效的光热转换能力和按需释药特性。转录组学分析进一步表明,该复合水凝胶还能激活PI3K-AKT和Wnt信号通路,在分子层面促进组织再生。在糖尿病小鼠皮肤全层缺损模型中,HPCT水凝胶在近红外激光照射下显著加速伤口愈合,通过减轻炎症和氧化应激、增强血管生成及改善胶原沉积,展现出优异的治疗效果和良好的生物相容性。综上所述,HPCT水凝胶为糖尿病及其他慢性创面的管理提供了一种有前景的多功能治疗策略。
核心研究亮点
1.药食同源活性成分姜黄素的创新性应用与协同递送
研究首次将药食同源活性成分姜黄素(经铜离子络合改性为Cur-Cu NPs)与Ti₃C₂ MXene纳米片共同负载于温敏双网络水凝胶(HPCT)中,构建了“抗氧化-抗炎-抗菌-促血管生成”多功能协同治疗平台。Cur-Cu NPs解决了姜黄素水溶性差、稳定性低的瓶颈问题,铜离子的引入进一步赋予其促血管生成功能;Ti3C2 MXene提供高效ROS/RNS清除、光热响应及物理抗菌性能;PNIPAM/HPC双网络水凝胶基质则实现按需释药。三者协同,实现了对糖尿病创面多重病理屏障的同步调控。
2. 光热响应按需释药与多重ROS/RNS清除能力的系统验证
研究系统表征了HPCT水凝胶的温敏相变特性:通过将相变温度提升至40℃以上,避免了生理温度下的非特异性收缩;在808 nm近红外激光照射下,水凝胶温度升高21.6 °C,触发体积收缩(35.9%)与重量损失(33.4%),实现Cur-Cu NPs与Ti3C2的高效按需释放(三次开关循环累积释放率达94.7%)。在抗氧化层面,Ti3C2 MXene在2.5 μg/mL超低浓度下即可几乎完全清除DPPH·、ABTS+及·OH,并展现出过氧化氢酶样活性(分解H2O2生成O2缓解缺氧)。细胞水平上,HPCT将H2O2诱导的胞内ROS水平降至对照组的40.1%,并将受氧化应激损伤的细胞存活率从42.9%提升至111.2%。
3. 转录组学与体内实验揭示的协同治疗机制及良好生物相容性
研究通过流式细胞术证实,HPCT水凝胶可显著逆转LPS诱导的巨噬细胞异常极化:CD86+ M1型比例从39.1%降至6.9%,CD206+ M2型比例从0.5%升至32.0%。RNA-seq及Western blot分析进一步揭示,Ti3C2激活PI3K-AKT通路(上调p-AKT),Cur-Cu NPs激活Wnt/β-catenin通路(上调c-Myc),两条通路的协同激活仅在HPCT组中观察到。在STZ诱导的糖尿病小鼠模型中,HPCT+NIR组第9天创面闭合率超过90%(PBS组仅55.9%),组织学分析显示CD31+新生血管率(10.1%)、α-SMA+成熟血管率(4.8%)及VEGF阳性率(68.63%)均为各组最高,同时促炎因子TNF-α和IL-1β分别降至对照组的1/6和1/11。安全性评价证实HPCT水凝胶细胞存活率>85%、溶血率<1.38%,主要脏器无异常,展现出良好的临床转化前景。
作者简介
第一作者

廖涛,博士,湖北工业大学生命科学与健康工程学院博士后。湖北工业大学生命科学与健康工程学院博士后。主要研究方向为生物医用高分子材料、智能纳米药物递送系统、多功能创面修复材料。主持发酵工程教育部重点实验室开放基金、湖北工业大学博士人才启动项目,并参与国家自然科学基金面上项目。在Journal of Nanobiotechnology、Acta Biomaterialia、Nano Research等国际知名期刊发表SCI论文33篇,其中以第一/共同第一作者发表13篇,个人相关学术成果聚焦临床关键问题的智能响应型诊疗系统构建,具备独立开展高水平科研的能力与扎实的实验技术。
通讯作者

匡映,博士,副教授,硕士生导师,湖北工业大学“南湖学者”、百优教师、生命科学与健康工程学院教学指导委员会委员,担任《Food & Medicine Homology》青年编委。主要研究方向为食源性大分子的分离纯化、结构化改造和分子互作机制研究,以及功能食品因子稳态化递送与体内定位控释。主持国家自然科学基金、中国博士后面上基金、湖北省自然科学基金等项目10余项,在Advanced Functional Materials、Nano today、Biomaterials等国际知名期刊发表SCI论文73篇(其中第一及通讯作者论文35篇),授权国家发明专利5项。获湖北省科技进步三等奖1项,世界可持续能源技术协会 (WSSET) 学术创新奖1项。个人H指数27,i-10指数47(基于Web of Science数据)。

李草,博士、教授,博士生导师,中国生物材料学会高级会员、湖北省药学会理事、武汉市青年科技晨光计划入选者、湖北工业大学高层次人才,主要研究方向为用于重大疾病诊疗的纳米药物。曾任湖北大学首届沙湖学者、湖北大学学术道德与仲裁专门委员会委员、健康科学与工程学院学位评定分委员会委员,现为湖北工业大学生命科学与健康工程学院院长助理、药学学科带头人。至今主持国家自然科学基金3项、省部级及其他项目10余项。在Advanced Functional Materials、Nano Today、Chemical Engineering Journal等国际学术期刊上发表SCI论文130余篇(其中第一及通讯作者论文60余篇),累计影响因子400多,H指数40,i-10指数90(基于Web of Science数据)。以第一发明人身份授权国家发明专利9项。担任期刊《Nano Materials Science》、《Nano Biomedicine and Engineering》、《Nano TransMed》、《Interdisciplinary Medicine》、《胶体与聚合物》青年编委。

刘佳,博士,湖北工业大学生命科学与健康工程学院教授、湖北省杰青、博士生导师。博士毕业于武汉大学-生物医用高分子材料教育部重点实验室,荷兰乌特勒支大学药学系联合培养。主要从事纳米药物和活性材料的研发,炎症、肿瘤及创伤等疾病的诊疗。主持国家自然科学基金3项、湖北省杰出青年基金及其他省部级项目多项。以第一/通讯作者发表SCI论文40篇(IF>10分24篇,ESI高被引论文2篇),包括Journal of the American Chemical Society、Advanced Functional Materials、Nano Today、Advanced Science和Biomaterials等高水平学术期刊;获得国家发明专利授权8项;获得湖北省科技进步一等奖和中国抗癌协会科技奖二等奖。
原文链接:https://doi.org/10.1186/s12951-026-04189-5
扫码关注我们吧
