
Introduction
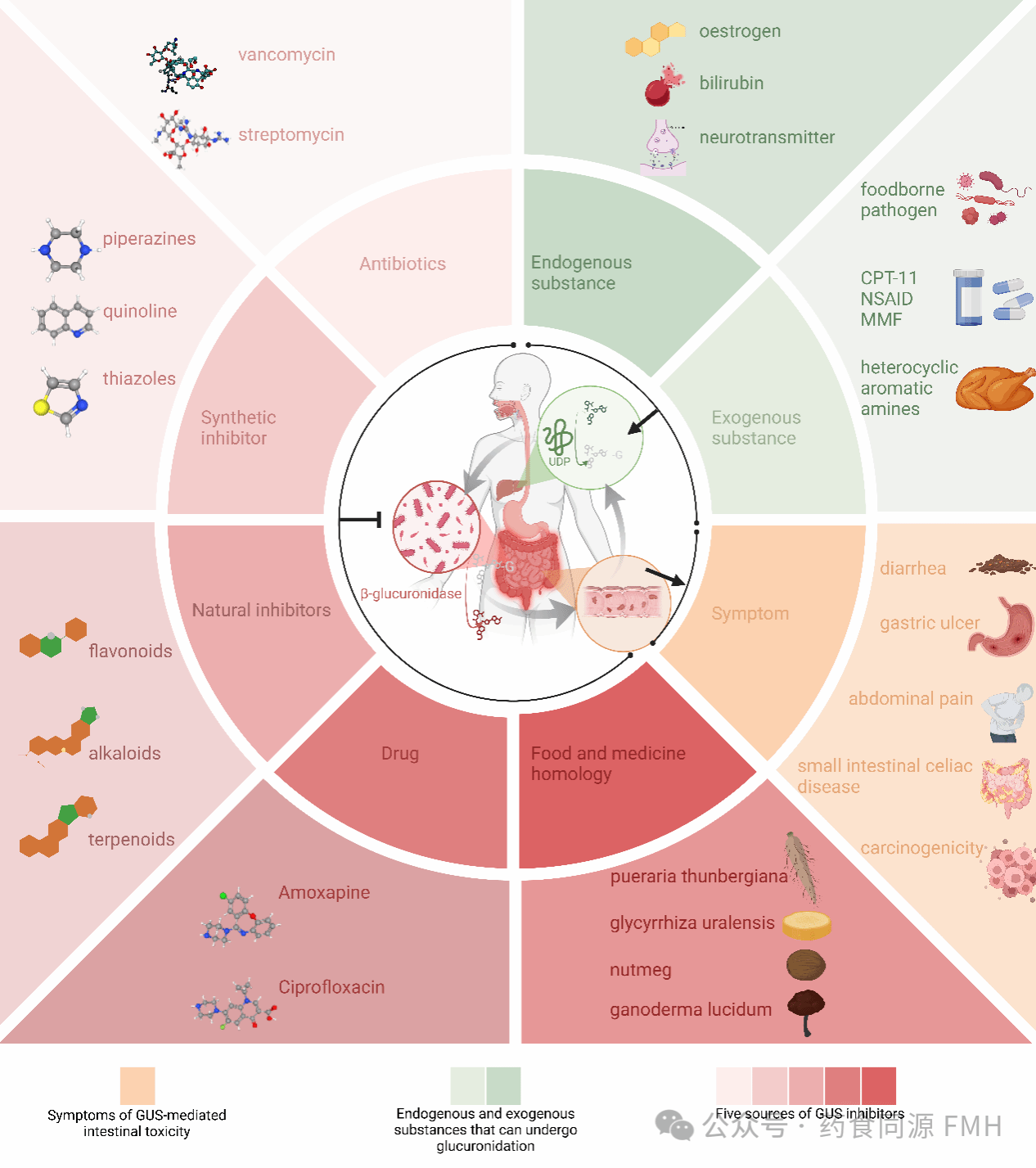
人类肠道菌群是一个复杂且动态的微生物生态系统,对维持宿主健康起着至关重要的作用。作为宿主-微生物共生体系的核心,肠道菌群具有高度的多样性并维持相对的稳定性。近年来,β-葡萄糖醛酸苷酶(β-glucuronidase, GUS)已成为肠道健康领域的研究热点。GUS广泛分布于人体自身组织及多种肠道微生物中,能够催化葡萄糖醛酸结合物的水解反应,释放出游离的外源性成分(如食源性危害物、药物等)或内源性代谢物,从而显著调节这些物质在肠道内的浓度与生物利用度。尽管GUS在功能成分的代谢转化、激素平衡调节等方面具有重要生理功能,但过高的酶活性也可能引发肠道毒性反应,成为影响食品安全、药物毒副作用的潜在风险因素。因此,本文系统综述GUS的生物学来源、结构特征与生理功能,探讨其介导肠道毒性的主要机制,分析影响GUS活性的关键因素,并重点阐述靶向GUS的干预策略及其在食品安全领域的应用前景,以期为食品营养与肠道健康的深入研究提供理论依据和实践参考。
Results and discussion
GUS酶的来源、结构与功能
GUS酶的来源多种多样,包括了动物、植物、细菌。在植物中,多种植物已被表征具有GUS酶活性,包括模式植物拟南芥、水稻、烟草和玉米等。近年关于GUS酶的研究主要聚焦于人体,人体中的GUS酶主要分为两个来源,一个是由人体自主产生的HGUS,一个是由人体肠道细菌产生的BGUS。HGUS是一种在许多组织和体液中表达的酸性水解酶。在人类肠道微生物群中GUS酶也分布广泛,特别是厚壁菌门(Firmicutes)、拟杆菌门(Bacteroidetes)、放线菌门(Actinobacteria)、酸杆菌门(Acidobacteria)和变形菌门(Proteobacteria)等细菌门中。GUS酶属于糖苷水解酶(Glycoside Hydrolase, GH)家族2族(GH2),其催化机制依赖于活性位点中的两个催化性谷氨酸残基(E413和E504),其主要功能是催化葡萄糖醛酸结合物的水解,而葡萄糖醛酸化过程涉及将葡萄糖醛酸(GlcA)分子结合到各种内源性和外源性化合物上,是促进这些物质通过胆汁和尿液排出、从体内清除的关键机制。
 2
2
GUS酶与肠道毒性
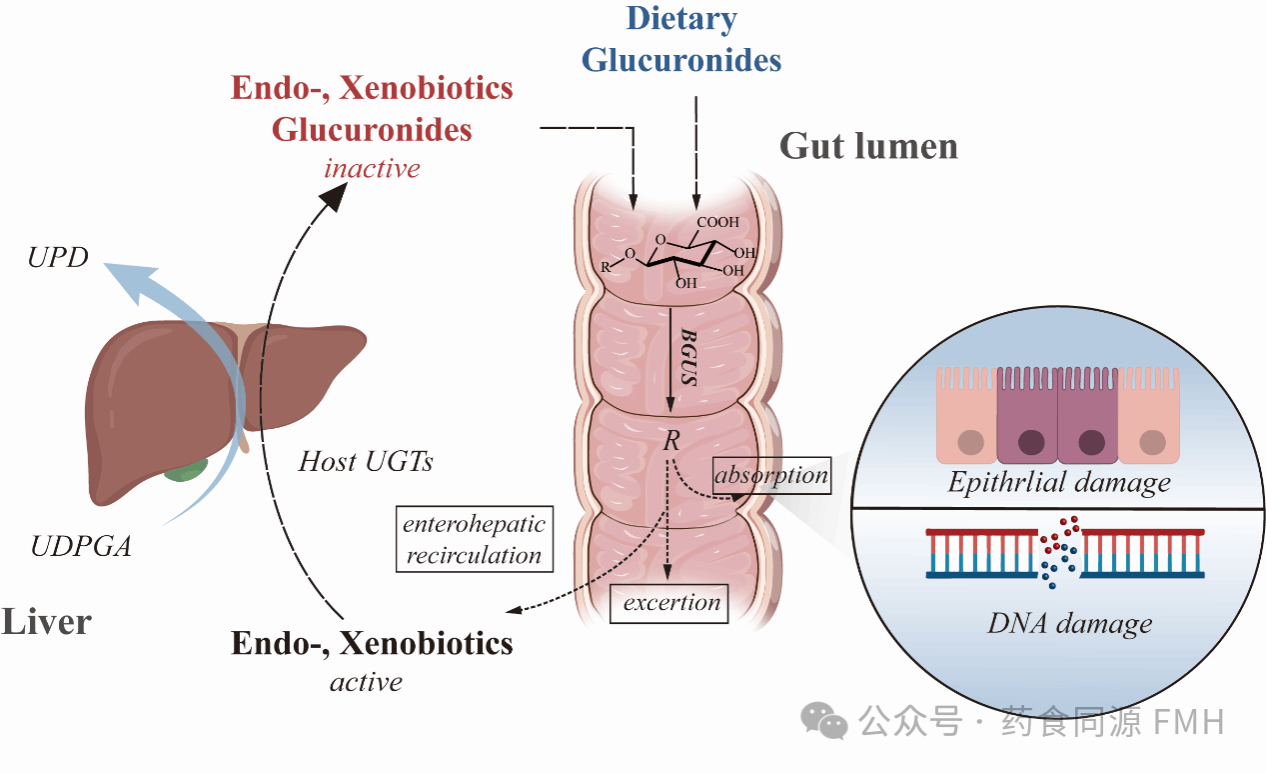
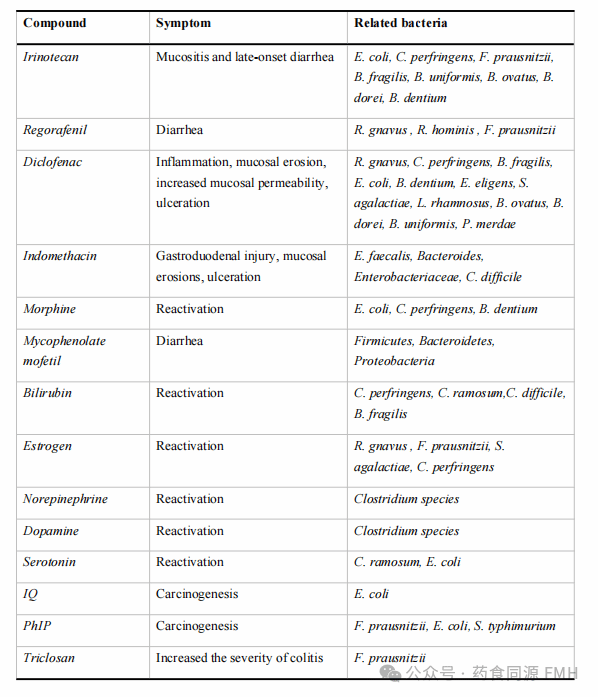
肠道菌群中的GUS能够分解葡萄糖醛酸,将其作为碳源利用。这一过程导致原本待排出的苷元在肠道中重新生成,它们可能重新进入血液循环,并参与肠肝循环,最终返回肝脏。值得注意的是,这些重新活化的苷元对肠道组织可能极具毒性,据研究显示,这些化合物在人体中可能引发严重的副作用。如药物、内源性代谢物、食源性危害物等产生的危害都与GUS相关。
伊立替康的前体药物在体内转化为SN38,这是一种强效的拓扑异构酶I抑制剂,能够减缓肿瘤细胞和每5天更新一次的肠道上皮细胞的快速增殖。SN38通过结合葡萄糖醛酸(GlcA)进行解毒,生成SN38-G,这是一种可通过消化道排出的物质。然而,肠道细菌产生的GUS能够从SN38-G中移除GlcA,使SN38重新活化,进而引发上皮细胞损伤,在动物模型中表现为出血性腹泻和急剧体重下降。
雌激素作为一种非常常见的内源性苷元,在人类中具有关键的生理作用,并且雌激素的过度暴露长期以来被认为是性激素反应性疾病如乳腺癌(BCa)的决定因素,GUS酶在内源性激素的代谢中扮演重要角色,尤其是雌激素类激素。在肠道中,GUS酶通过去除雌激素-葡萄糖醛酸结合物,释放游离的激素形式,这些自由激素进入肠道和血液循环,可能导致雌激素水平的异常升高。这种激素的积累与乳腺癌等激素依赖性肿瘤的发生密切相关。
食源致病菌可以导致细菌性腹泻和急性肠胃炎。食源致病菌的入侵可能会破坏肠道内益生菌和有害菌之间的平衡,导致益生菌减少,有害菌大量繁殖,分泌大量毒素,影响机体免疫力,引发腹胀腹泻、肠炎甚至各种慢性代谢性疾病。近期有研究发现,通过GUS抑制,减少肠道中游离葡萄糖醛酸的释放,可减少肠道致病菌摄取游离葡萄糖醛酸作为碳源,减少致病菌定殖。
影响GUS酶活性的关键因素
GUS酶活性在不同环境和条件下表现出显著的变化,受多种内外部因素的调节。肠道菌群的组成对GUS酶的活性有重要影响。不同的肠道微生物群体具有不同的GUS酶亚型和活性水平,且这些微生物群体的动态变化可能直接影响GUS酶的表达和功能。肠道微生物群中不同菌种的GUS酶亚型(如L1型、L2型、NL型等)具有不同的底物特异性和催化效率。食物成分、饮食习惯以及环境污染物都会影响肠道微生物群的组成,进而调控GUS酶的活性。高脂肪饮食(特别是动物脂肪)被发现可显著增加GUS酶的活性。宿主的年龄、性别、遗传背景等生理特征,以及其健康状态,都对GUS酶的活性具有调控作用。
以GUS酶为靶标的毒性消减策略
有效的GUS抑制剂可以调节肠道细菌GUS活性,从而减轻某些异生素的肠道毒性或预防结肠相关疾病。因此,GUS抑制已成为一种管理疾病和药物治疗的新方法,并引起了越来越多的研究兴趣。抗生素的使用在减轻肠道细菌GUS介导的药物毒性方面有一些益处,然而,广谱抗生素的使用是不加选择地消除大量的肠道共生细菌,抗生素在杀灭病原菌的同时,也会影响肠道中的共生菌,导致肠道微生物群的组成和功能发生改变,长期使用抗生素可能导致肠道微生物群的长期变化,这些变化可能与多种疾病的风险增加有关,包括过敏、代谢、免疫和炎症性疾病。现在常用作研究GUS的抑制剂来源主要分为两部分,一方面是合成的抑制剂,另一方面药用植物中的天然化合物也是发现先导化合物或候选药物的主要来源。
在合成抑制剂方面虽然进行了大量的新抑制剂合成,但合成抑制剂能够真正应用到临床需要大量验证,用时久远。虽然一些已知药物,被发现具有GUS抑制的作用。但药物联用是否会引起其他副作用,需要进一步挖掘。总体来讲,天然来源GUS抑制剂,尤其是药食同源药材中的天然化合物,拥有较强的优势,但如何得到高效的GUS抑制剂以及广谱/特定的GUS抑制剂,是接下来的研究方向。
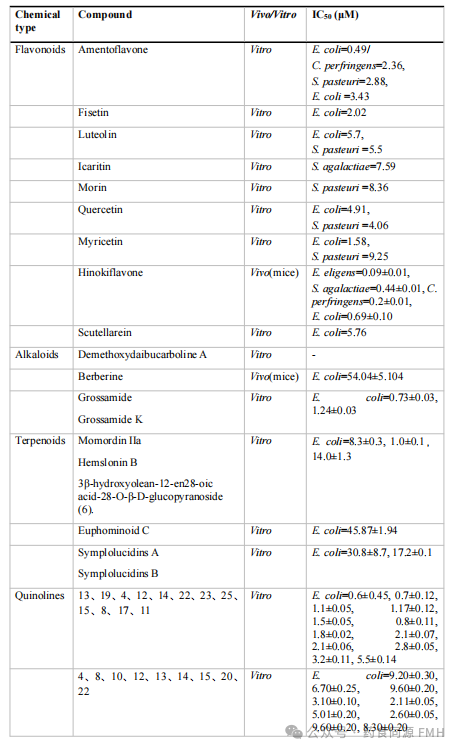
药食同源来源的化合物作为GUS抑制剂的前景
现有抑制剂多只使用EcoGUS进行筛选,虽然EcoGUS是肠道中最主要的GUS之一,但在不同的疾病条件下,肠道菌群丰度会随之变化,在不同病理状态下,参与代谢过程的GUS可能不同,并且GUS还参与体内内源化合物的代谢,而这些内源化合物维持着日常的生理活动。因此发现特定病理过程发挥作用的GUS以及针对性特异抑制剂,对抑制剂的高效利用以及正常生理活动的维持都具有重要作用。药食同源来源的化合物的优势之一就是化合物种类众多,已有化合物基础强大,不需要重设计结构。通过在大量药食同源来源的天然化合物中进行虚拟筛选,缩小范围后,就能有机会发现有效抑制剂,甚至不止一种抑制剂。最后,将每种疾病状态与GUS酶和抑制剂连接起来,形成疾病-特异GUS-特异性抑制剂的一对一关系,做到精准抑制。
从肉豆蔻中分离的脱氢二异丁香酚(DDIE)通过改善体重减轻、结肠缩短、上皮屏障功能障碍、杯状细胞和肠道干细胞(ISC)损失和伤口愈合,同时DDIE对抗CPT11诱导的粪肠球菌增加,导致肠道Gus和SN38水平降低。减轻CPT11诱导的肠粘膜炎,同时与 CPT11协同抗肿瘤作用。这就证明了天然抑制剂作为GUS抑制剂,所具备的的多层次治疗作用,从疾病的各个方面都能介入治疗。为相关疾病治疗展示出了更好的预后效果。
Conclusion
合成抑制剂在临床应用中面临诸多挑战,包括安全性、特异性及副作用等问题。随着临床对GUS抑制剂的需求日益增长,天然抑制剂,尤其是源自药用植物的抑制剂已成为最具前景的解决方案。然而,天然化合物的筛选与开发工作仍不完善,许多具有生物活性的化合物尚未得到充分探索。此外,尽管GUS酶在多种生理过程中发挥关键作用,但其许多功能仍未被充分认知,其在其他生理与病理通路中的参与机制也有待进一步研究。宏基因组测序、细菌培养和虚拟筛选技术的进步已成为发现GUS抑制剂的关键驱动力,为寻找新治疗靶点提供了助力。然而,针对特定GUS酶的精准发现仍处于早期阶段,需要更深入的研究与优化。迄今为止,大多数关于GUS抑制的研究主要在体外或动物模型中进行,这些成果并不都能直接转化为临床应用。开发具有显著药理特性的GUS抑制剂对于降低靶向药物治疗中由GUS引起的毒性至关重要。最后,为从海量化合物中筛选出高效抑制剂,并阐明GUS在特定生理过程中的作用,计算学方法也可提供高效系统的解决方案。分子对接、虚拟筛选、机器学习及人工智能驱动的药物发现等技术,能够加速潜在GUS抑制剂的识别,并深化我们对酶-底物相互作用的理解,从而为靶向治疗策略的制定开辟道路。
作者简介
第一作者

郭宇恒,女,中国药科大学2025级博士研究生,主要研究方向为膳食成分与肠道微生物酶互作的机制挖掘。
通讯作者

程抒劼,副教授,博士生导师,美国印第安纳大学健康医学中心博士后。现任职于中国药科大学工学院食品营养与安全系/国家中药材加工技术研发专业中心。先后主持国家自然科学基金、“十四五”国家重点研发计划“食品营养与安全关键技术研发” 重点专项子课题、山东省重点研发计划子课题、江苏省自然科学基金、江苏省农业科技自主创新项目、拉萨市重大科技计划项目、校企合作项目等科研项目10余项。近年来以第一作者或/和通讯作者在Journal of Agricultural and Food Chemistry、Food & Function、International Journal of Biological Macromolecules、Nanoscale 等SCI 收录期刊上发表相关论文20余篇,获授权发明专利5项。担任国家自然科学基金函评专家、江苏省老年学学会老年营养专委会委员、江苏省食品学会青年委员会委员以及多个 SCI期刊审稿人。
论文网址:https://www.sciopen.com/article/10.26599/FMH.2026.9420139
欢迎关注我们
